Weiter Diskussion um „Sonstige Produkte zur Wundbehandlung“
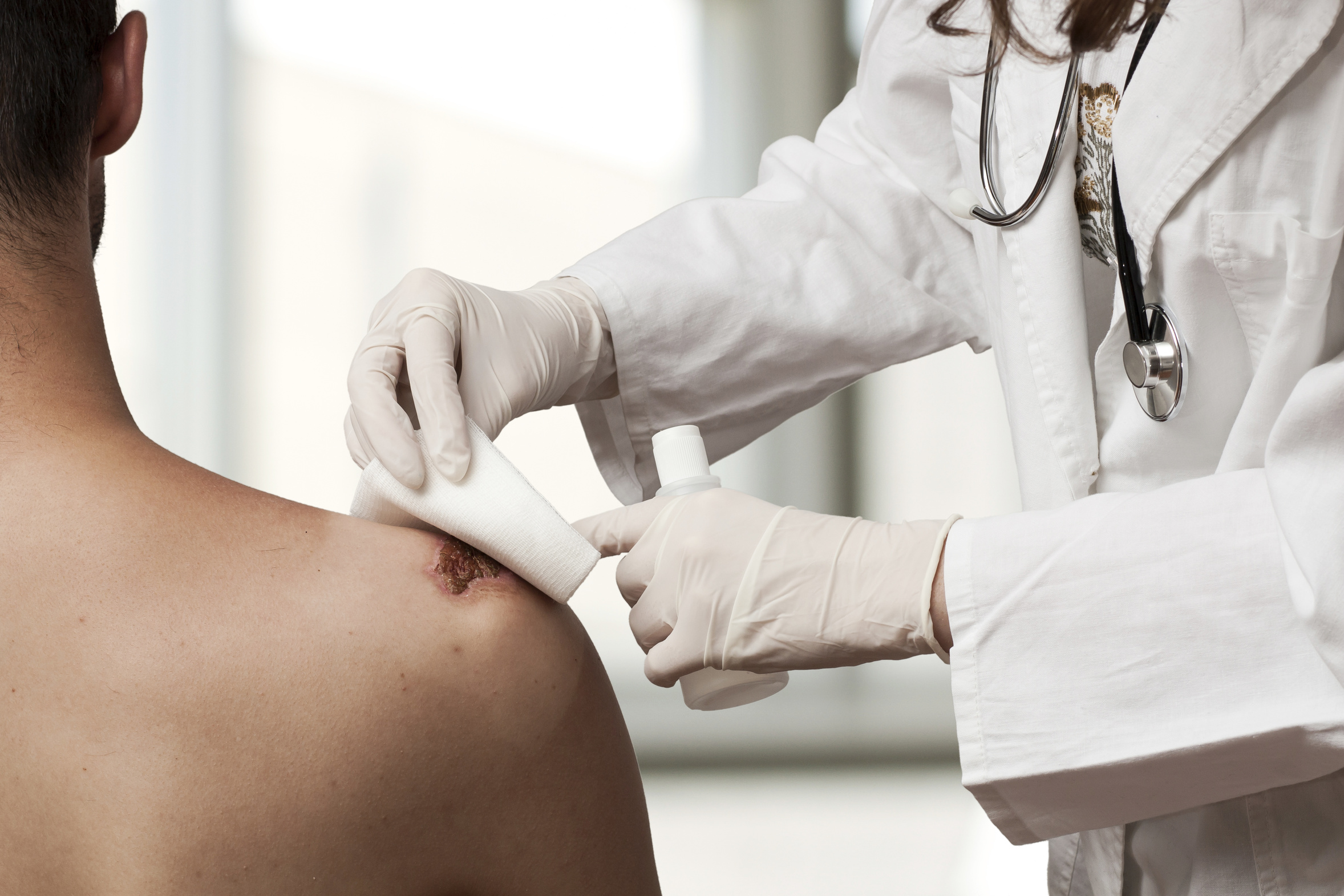
Hintergrund: Für die Erstattung der „Sonstigen Produkte zur Wundbehandlung“ endet Anfang Dezember 2024 eine Übergangsfrist. Um danach noch in der Gesetzlichen Krankenversicherung (GKV) erstattungsfähig zu sein, müssen sie gesonderte Nutzennachweise (Evidenz) erbringen.
Viele Wundauflagen aktuell im Krisenmodus
Betroffen sind davon u. a. antimikrobielle Wundauflagen für chronische Wunden (wir berichteten mehrfach). Evidenz sei „sehr wichtig“, betonte Juliane Pohl, Leiterin des Referats Ambulante Gesundheitsversorgung beim BVMed, allerdings funktioniere der für den Nutzennachweis notwendige Prozess beim Gemeinsamen Bundesausschuss (G-BA) bisher nicht.
Sie erinnerte daran, dass den betroffenen Verbandmittel-Herstellern zwar ein Beratungsrecht zu den Methoden der für die Nutzenbewertung erforderlichen Studien eingeräumt wurde. Das Problem dabei: Bislang sind in der G-BA-Praxis keine auf die Wundversorgung angepassten Evidenzkriterien definiert.
Wundverschluss nicht alleinige Zweckbestimmung
Hinzu komme als grundsätzliches Problem in der ganzen Diskussion, dass als sogenannter Endpunkt der Behandlung der vollständige Wundverschluss vorgesehen sei, erläuterte Pohl. Die betroffenen Produkte hätten aber eine andere Zweckbestimmung und seien oft nur für die temporäre Anwendung vorgesehen. Ergo könnten sie den Nutzennachweis des Wundverschlusses gar nicht erbringen, weil sie dafür weder vorgesehen seien noch verwendet würden.
Erneute Fristverlängerung möglich
Gleichwohl zeigte sich die BVMed-Vertreterin optimistisch, denn nun habe der G-BA wohl doch verstanden, dass für diese Produkte die „richtigen Endpunkte“ gefunden werden müssten.
Sie verwies auf ein Interview des G-BA-Vorsitzenden Prof. Josef Hecken mit der „ÄrzteZeitung“, wonach bei der Verbandmittel-Erstattung politischer Handlungsbedarf bestehe (wir berichteten; MTD-Instant KW 21). Damit habe er auf politischer Ebene eine Diskussion in Gang gebracht.
Das vom G-BA beauftragte IQWIG solle nun in den kommenden zehn Monaten die genauen Kriterien klären. Indessen forderte der BVMed mit Blick auf diesen Zeitraum postwendend eine erneute Verlängerung der im Dezember 2024 auslaufenden Frist.
Ihnen hat dieser Artikelauszug gefallen? Dann lernen Sie den wöchentlich erscheinenden Branchen-Informationsdienst „MTD-Instant“ noch besser kennen. Bestellen Sie jetzt Ihr Test-Abonnement.
Ihnen hat dieser Artikel gefallen? Dann lernen Sie das Fachmagazin MTD Medizintechnischer Dialog noch besser kennen. Bestellen Sie jetzt Ihr Test-Abonnement.